Sare. Bicarbonat de amoniu
Ce este sarea?
O clasă de compuși chimici care conțin un cation metalic sau un cation de amoniu conectat la un anion sub formă de reziduu acid are numele comun - săruri. Ele sunt împărțite în mediu (sau mediu), acid, bazic, dublu, hidratat (hidraturi cristaline), complex.
Sărurile normale (sau medii) sunt caracterizate printr-o înlocuire completă a cationilor de hidrogen în molecula de acid cu un cation metalic sau de amoniu, de exemplu: sulfat de sodiu Na2S04 sau carbonat de calciu CaC03.
În cazul în care molecula de acid cationilor de hidrogen parțial substituit cu un cation, astfel de săruri acide sunt numite, de exemplu, NH4HCO3 bicarbonat de amoniu sau carbonat acid de sodiu NaHCO3.
Dacă molecula de bază nu a fost completă și substituția parțială a grupărilor hidroxil pe radicalul de acid, sărurile formate sunt numite de bază, de exemplu, digidroksokarbonat cupru (CuOH) 2CO3.
În formula sărurilor duble există două cationi diferiți, de exemplu, aluminiul și potasiul în alum-aluminiu de potasiu KAl (SO4) 2 • 12 H2O.
Formula de săruri amestecate conține doi anioni diferiți, de exemplu, clorura de calciu (OCI).
Compoziția moleculelor de săruri de hidrat include apă de cristalizare, de exemplu, sulfat de cupru (albastru) CuS04.5H20.
Moleculele constau din săruri complexe sau complexe cation anion complex, de exemplu, clorură de tetraammintsinka (II) [(Zn (NH3) 4)] CI2.
Cum se formează numele sărurilor?
Există două cuvinte în numele sărurilor. Primul este numele anionului, care se află în cazul nominativ. Al doilea cuvânt (în cazul genitiv) derivă din numele cationului. De exemplu: sulfat de sodiu Na2S04, sulfat de fier (II) FeS04, sulfat de fier (III) Fe2 (S04) 3, carbonat de calciu CaC03, clorură de cupru CuCI2. În numele sărurilor acide, înaintea denumirii anionului, se scrie prefixul "hidro;" sau prefixul "bi;", dacă rămâne un cation hidrogen nesubstituit în moleculă. Dacă există două astfel de cationi de hidrogen, prefixul "dihidro;" este scris înaintea numelui anionului. Exemple: bicarbonat (sau bicarbonat) de NaHCO3 de sodiu (această sare se numește și bicarbonat de sodiu), dihidrogenfosfat de sodiu NaH2PO4.
Bicarbonat de amoniu. formulă
In formula sare de acid carbonic acid NH4HCO3, în care cationul de amoniu este inclus, de asemenea, anion HCO3- format prin substituirea parțială în molecula de cation hidrogen acid la ionul de amoniu încărcat pozitiv. Adică molecula acestei săruri acide constă dintr-un cation de amoniu NH4 + legat la un anion, care poartă numele de HCO3-. Formula brută pentru sistemul Hill este scrisă ca: CH5NO3. Greutatea moleculară a substanței este de 79,06 a. e. m.
proprietăţi
Bicarbonatul de amoniu este un compus anorganic, în chip de cristale incolore, cu o latură rombică. Densitatea este de 1,586 g / cm3 (la 20 ° C). Presiunea de vapori crește: de la 59 mm. Hg. Art. (la 25,4 ° C) până la 278 mm. Hg. Art. (la 45 ° C).
Bicarbonatul de amoniu nu se dizolvă în alcool etilic și acetonă. Se dizolvă ușor în apă: cu o temperatură în creștere, solubilitatea sării acide crește de la 11,9 g / 100 g (la 0 ° C) la 36,6 g / 100 g (la 40 ° C).
Bicarbonatul de amoniu se descompune prin eliberarea de CO2 deja la 20 ° C. La o temperatură de 36-70 ° C, sarea se descompune în soluții apoase. Ca rezultat, se eliberează amoniac, se formează apă și dioxid de carbon: NH4HCO3 → NH3 uarr- + CO2 uarr- + H2O.
Datorită hidrolizei, soluția apoasă are o reacție ușor alcalină. Când se adaugă concentrat soluție de amoniac se formează o sare normală: NH4HCO3 + NH3 - (NH4) 2CO3.
Sub influența acizilor și a alcaliilor, sarea acidă este distrusă reacții: NH4HCO3 + HCI → NH4CI + CO2uarr- + H20 sau NH4HCO3 + 2 NaOH → Na2C03 + NH3 • H20 + H20.
Bicarbonat de amoniu. recepție
Ca toate hidrogencarbonați, sare de acid de amoniu se poate obține printr-un dioxid de carbon trece lung prin soluția secundară de sare de amoniu: (NH4) 2CO3 + CO2 + H2O → 2 NH4HCO3.
Atunci când sarea de mijloc este ușor încălzită (30 ° C), descompunerea sa termică la sare acidă și amoniac are loc: (NH4) 2CO3 → 2 NH4HCO3 + NH3.
Dacă apa dizolvă dioxidul de carbon și amoniacul, este de asemenea posibil să se obțină o sare acidă de amoniu: NH3 + CO2 + H2O → NH4HCO3.
cerere
Bicarbonatul de amoniu este utilizat pe scară largă în industria alimentară: acesta joacă rolul unei pulberi chimice de copt pentru producerea de produse de cofetărie și de făină. Se știe că bicarbonatul de sodiu NaHC03 este, de asemenea, utilizat pentru a ridica aluatul fără plumb. Dar utilizarea sa este mai puțin eficientă, deoarece strângerea frământării sau înmuiere până când coacerea duce la o îndepărtare mai rapidă a dioxidului de carbon format ca urmare a reacției cu acidul, iar aluatul în acest caz nu va fi luxuriant și ușor.
bicarbonatul de amoniu este utilizat pentru tăbăcirea și vopsirea materialelor textile: un proces de îndepărtare a colorantului nefixat (sau striperul) este un amestec de săruri de amoniu includ bicarbonat de amoniu.
Substanța este folosită în agricultură ca conservant al furajelor (procesele de dezintegrare se încetinesc, crescând astfel siguranța), precum și îngrășămintele pentru cartofi, culturi furajere și legume. Proprietățile sale sunt utilizate pentru încetinirea sau stoparea proceselor de nitrificare a solurilor.
Bicarbonatul de amoniu este utilizat în mineritul uraniu, în industria metalurgică, precum și în medicină (în producția de vitamine). În sinteza organică, servește ca materie primă pentru producerea de reactivi chimici, de exemplu, săruri de amoniu.
 Disocierea sărurilor, acizilor și alcalinilor. Teoria și aplicarea practică
Disocierea sărurilor, acizilor și alcalinilor. Teoria și aplicarea practică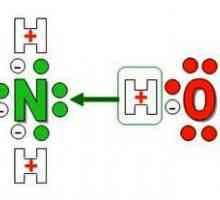 Apă de amoniac: preparat, formulă, aplicare
Apă de amoniac: preparat, formulă, aplicare Conceptul de hidroliză. Caracteristicile numerice ale procesului: constanta de hidroliză și gradul…
Conceptul de hidroliză. Caracteristicile numerice ale procesului: constanta de hidroliză și gradul… Chile saltpeter: o formulă și proprietăți. Formula chimică a azotatului de amoniu
Chile saltpeter: o formulă și proprietăți. Formula chimică a azotatului de amoniu Carbonat de sodiu, bicarbonat de sodiu - cel mai interesant
Carbonat de sodiu, bicarbonat de sodiu - cel mai interesant Sare de amoniu - metode de producție, utilizare în economia națională
Sare de amoniu - metode de producție, utilizare în economia națională Sulfuri și hidrosulfuri. Hidrosulfură și sulfură de amoniu
Sulfuri și hidrosulfuri. Hidrosulfură și sulfură de amoniu Substanțe anorganice
Substanțe anorganice Săruri duble: exemple și nume
Săruri duble: exemple și nume Sare de carbon de amoniu: descriere, compoziție, domeniu de aplicare
Sare de carbon de amoniu: descriere, compoziție, domeniu de aplicare Reacții calitative
Reacții calitative Hidroliza: ecuația moleculară și ionică. Ecuația reacției de hidroliză
Hidroliza: ecuația moleculară și ionică. Ecuația reacției de hidroliză Clase de compuși anorganici
Clase de compuși anorganici Acid carboxilic
Acid carboxilic Sare acide
Sare acide Oxizi amfoterici. Proprietăți chimice, metoda de producție
Oxizi amfoterici. Proprietăți chimice, metoda de producție Acid hidrobromic. Metode de preparare, proprietăți fizice și chimice
Acid hidrobromic. Metode de preparare, proprietăți fizice și chimice Hidroxid de magneziu. Proprietăți fizice și chimice. Aplicație.
Hidroxid de magneziu. Proprietăți fizice și chimice. Aplicație. Proprietăți chimice ale sărurilor și metode de preparare a acestora
Proprietăți chimice ale sărurilor și metode de preparare a acestora Bicarbonat de magneziu: proprietăți fizice și chimice
Bicarbonat de magneziu: proprietăți fizice și chimice Amoniu este un ion de interacțiune donor-acceptor
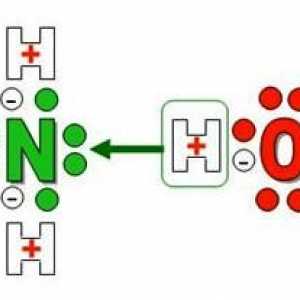
Amoniu este un ion de interacțiune donor-acceptor
 Apă de amoniac: preparat, formulă, aplicare
Apă de amoniac: preparat, formulă, aplicare Chile saltpeter: o formulă și proprietăți. Formula chimică a azotatului de amoniu
Chile saltpeter: o formulă și proprietăți. Formula chimică a azotatului de amoniu Săruri duble: exemple și nume
Săruri duble: exemple și nume Sare de carbon de amoniu: descriere, compoziție, domeniu de aplicare
Sare de carbon de amoniu: descriere, compoziție, domeniu de aplicare