Regula Markovnikova V. V. Esență și exemple
În reacțiile chimice în locul distrugerii dublei legături în alchene și triple în alchine, pot fi atașate diferite particule. Care sunt legile care guvernează acest proces? Comportamentul omologilor asimetrici ai etilenei în timpul hidrohalogenării și hidratării a fost studiat de omologul rus VV Markovnikov. El a descoperit că mecanismul reacției depinde de cantitatea de hidrogen legată de carbonul din legătura dublă. Ipoteza avansată de om de știință a fost confirmată după descoperirile din teren structura atomului. Regula de la Markovnikov a pus bazele creării unei teorii științifice care are o aplicație practică. Permite organizarea mai rațională a producției de polimeri, lubrifianți, alcooli.
conținut

Regula lui Markovnikov
Cercetătorul rus sa dedicat mult timp studierii mecanismului de atașare a reactivilor asimetrici la hidrocarburi nesaturate. În articolul său, publicat în limba germană în 1870, VV Markovnikov a atras atenția comunității științifice asupra selectivității interacțiunii dintre halogenurile de hidrogen cu atomi de carbon situate la legătura dublă din alchene nesimetrice. Cercetătorul rus citează datele pe care le obținuse experimental în laboratorul său. Markovnikov a scris că halogenul se alătură în mod necesar atomului de carbon care conține cea mai mică cantitate atomi de hidrogen. O mare popularitate a muncii omului de știință a fost dobândită la începutul secolului al XX-lea. Ipoteza mecanismului de interacțiune propus de el era numită regula lui Markovnikov.
Viața și munca unui om de știință ecologic
 Vladimir Vasil`evich Markovnikov sa născut la 25 decembrie 1837 (în stil în stilul St Petersburg). A studiat la Universitatea din Kazan, a predat mai târziu la această școală și la Universitatea din Moscova. Markovnikov a studiat comportamentul hidrocarburilor nesaturate în interacțiune cu halogenurile de hidrogen din 1864. Până în 1899, oamenii de știință din alte țări nu au acordat importanță concluziilor Chimist rus. Markovnikov, pe lângă regula, numită în onoarea sa, a făcut o serie de alte descoperiri:
Vladimir Vasil`evich Markovnikov sa născut la 25 decembrie 1837 (în stil în stilul St Petersburg). A studiat la Universitatea din Kazan, a predat mai târziu la această școală și la Universitatea din Moscova. Markovnikov a studiat comportamentul hidrocarburilor nesaturate în interacțiune cu halogenurile de hidrogen din 1864. Până în 1899, oamenii de știință din alte țări nu au acordat importanță concluziilor Chimist rus. Markovnikov, pe lângă regula, numită în onoarea sa, a făcut o serie de alte descoperiri:
- a primit acid ciclobutandicarboxilic;
- a investigat petrolul din Caucaz și a descoperit în el substanțe organice de o compoziție specială - nafteni;
- a stabilit diferența în temperaturile de topire ale compușilor cu lanțuri ramificate și rectilinii;
- a demonstrat izomerismul acizilor grași.
Lucrările omului de știință au contribuit în mare măsură la dezvoltarea științei chimice interne și a industriei.
Esența ipotezei propuse de Markovnikov
Omul de știință a dedicat mulți ani studiului reacțiilor de adăugare a reactivilor la hidrocarburi nesaturate cu o dublă legătură (alkenuri). El a menționat că dacă hidrogenul este prezent în compuși, atunci acesta este direcționat către acel atom de carbon, care conține mai multe particule de acest fel. Anionul se alătură carbonului adiacent. Aceasta este regula lui Markovnikov, esența lui. Omul de știință a prezis în mod strălucit comportamentul particulelor, structura cărora încă nu avea idei foarte clare. În conformitate cu regula, substanțele complexe având compoziția de HX sunt adăugate la hidrocarburile etilenei, unde X:
- halogen;
- OH;
- reziduu acid de acid sulfuric;
- alte particule.
sunet regula Modern Markovnikov diferă de formulările de știință: un atom de hidrogen de la NH molecule alchena atașabilă este direcționat spre dublă legătură carbon la care conține deja mai hidrogen, iar X este particula se duce la cel mai mic atom hidrogenată.

Mecanismul de atașare a particulelor electrofile
Luați în considerare tipurile de transformări chimice în care se aplică regula Markovnikov. exemple:
- Reacția de adiție la hidrogen clorură de propen. În timpul interacțiunii dintre particule, legătura dublă se descompune. Anionul cloric este trimis la carbonul mai puțin hidrogenat care se găsește în legătura dublă. Hidrogenul interacționează cu cel mai hidrogenat dintre acești atomi. Forme de 2-clor propan.

- În reacția de adiție a moleculei de apă, hidroxilul din compoziția sa este adecvat pentru un carbon mai puțin hidrogenat. Hidrogenul este atașat la cel mai hidrogenat atom cu o legătură dublă.
Există excepții de la regula propusă de Markovnikov în acele reacții în care alchenele acționează ca reactivi, în care carbonul din legătura dublă are deja un număr de grupuri electronegative. Selectează parțial densitatea electronică la care este atras de obicei hidrogenul încărcat pozitiv. De asemenea, regula nu este observată în reacțiile care se desfășoară de-a lungul unui mecanism radical, mai degrabă decât electrofil, (efectul Harish). Aceste excepții nu distrug meritele regulii derivate de la chimistul rus organic V. V. Markovnikov.
 Alcadiene: proprietăți fizice, proprietăți chimice și aplicarea lor. Proprietățile fizice ale…
Alcadiene: proprietăți fizice, proprietăți chimice și aplicarea lor. Proprietățile fizice ale… Primul reprezentant al alkenelor este etilenă. Proprietățile fizice, producția, aplicarea etilenei
Primul reprezentant al alkenelor este etilenă. Proprietățile fizice, producția, aplicarea etilenei Formula benzenului: care dintre variante este corectă?
Formula benzenului: care dintre variante este corectă? Hidrocarburile sunt ... hidrocarburi finale. Clasele de hidrocarburi
Hidrocarburile sunt ... hidrocarburi finale. Clasele de hidrocarburi Metode de producere a alchenelor: laborator și industrial
Metode de producere a alchenelor: laborator și industrial Chimiști renumiți ruși, contribuția lor la știință
Chimiști renumiți ruși, contribuția lor la știință Formula generală a alchenelor. Proprietățile și caracteristicile alkenelor
Formula generală a alchenelor. Proprietățile și caracteristicile alkenelor Mari chimisti ai lumii si munca lor
Mari chimisti ai lumii si munca lor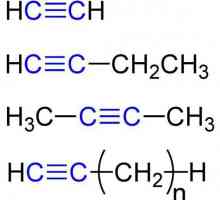 Proprietăți chimice ale alchinelor. Structura, recepția, aplicarea
Proprietăți chimice ale alchinelor. Structura, recepția, aplicarea Reacții calitative la alchene. Proprietăți chimice și structura alchenelor
Reacții calitative la alchene. Proprietăți chimice și structura alchenelor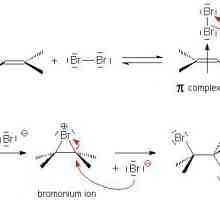 Adăugarea electrofilă în chimia organică
Adăugarea electrofilă în chimia organică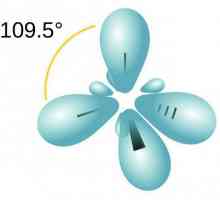 Să vorbim despre cum să determinăm tipul de hibridizare
Să vorbim despre cum să determinăm tipul de hibridizare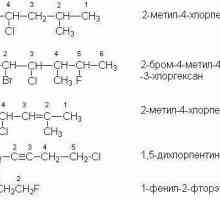 Ce este o nomenclatură sistematică
Ce este o nomenclatură sistematică Sunt hidrocarburile alifatice?
Sunt hidrocarburile alifatice? Hidrocarburi limită: caracteristici generale, izomerie, proprietăți chimice
Hidrocarburi limită: caracteristici generale, izomerie, proprietăți chimice Seria de omologie
Seria de omologie Hidrocarburi nesaturate: alcene, proprietăți chimice și aplicații
Hidrocarburi nesaturate: alcene, proprietăți chimice și aplicații Factorii care afectează rata de reacție chimică
Factorii care afectează rata de reacție chimică Proprietăți chimice ale alchenelor (olefine)
Proprietăți chimice ale alchenelor (olefine) Alkines: producție, aplicare, proprietăți
Alkines: producție, aplicare, proprietăți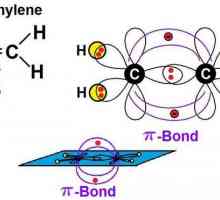 Alkenes: formula. Proprietăți chimice. recepție
Alkenes: formula. Proprietăți chimice. recepție
 Primul reprezentant al alkenelor este etilenă. Proprietățile fizice, producția, aplicarea etilenei
Primul reprezentant al alkenelor este etilenă. Proprietățile fizice, producția, aplicarea etilenei Formula benzenului: care dintre variante este corectă?
Formula benzenului: care dintre variante este corectă? Hidrocarburile sunt ... hidrocarburi finale. Clasele de hidrocarburi
Hidrocarburile sunt ... hidrocarburi finale. Clasele de hidrocarburi Metode de producere a alchenelor: laborator și industrial
Metode de producere a alchenelor: laborator și industrial Chimiști renumiți ruși, contribuția lor la știință
Chimiști renumiți ruși, contribuția lor la știință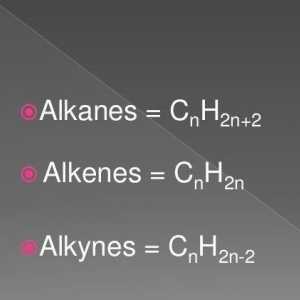 Formula generală a alchenelor. Proprietățile și caracteristicile alkenelor
Formula generală a alchenelor. Proprietățile și caracteristicile alkenelor Mari chimisti ai lumii si munca lor
Mari chimisti ai lumii si munca lor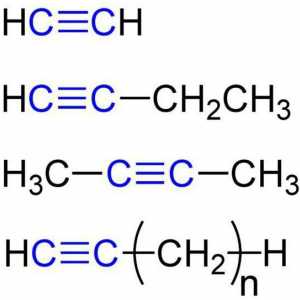 Proprietăți chimice ale alchinelor. Structura, recepția, aplicarea
Proprietăți chimice ale alchinelor. Structura, recepția, aplicarea Reacții calitative la alchene. Proprietăți chimice și structura alchenelor
Reacții calitative la alchene. Proprietăți chimice și structura alchenelor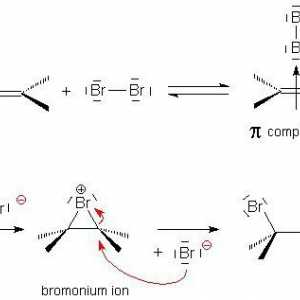 Adăugarea electrofilă în chimia organică
Adăugarea electrofilă în chimia organică