Formula generală a aminoacizilor
Aminoacizii, ale căror formule sunt considerate în cursul liceului, sunt substanțe importante pentru corpul uman. Proteinele, constând din reziduuri de aminoacizi, sunt necesare pentru ca o persoană să trăiască pe deplin.
conținut

definiție
Aminoacizii, ale căror formule vor fi considerate mai jos, sunt compuși organici în care moleculele conțin grupări amino și carboxil. Carboxilul constă dintr-un radical carbonil și hidroxil.
Puteți lua în considerare aminoacizii ca derivați ai acizilor carboxilici, în care atomul de hidrogen este înlocuit cu o grupare amino.

Caracteristicile proprietăților chimice
Aminoacizii, formula generală a căruia pot fi reprezentați ca CnH2nNH2COOH, sunt compuși chimici amfoterici.
Prezența a două grupări funcționale în moleculele lor explică posibilitatea manifestării de către aceste substanțe organice a proprietăților de bază și acide.
Soluțiile lor apoase au proprietățile soluțiilor tampon. Zwitterionul este o moleculă de aminoacizi, în care gruparea amino este NH3 +, iar carboxilul este reprezentat ca -COO-. O moleculă de acest tip are un moment dipol esențial, încărcarea totală fiind egală cu zero. Pe astfel de molecule sunt construite cristale de mulți aminoacizi.
Dintre cele mai importante proprietăți chimice ale acestei clase de substanțe, se pot identifica procese de policondensare care au ca rezultat formarea de poliamide, inclusiv proteine, peptide și nailon.
Aminoacizii, formula generală având forma CnH2nNH2COOH, reacționează cu acizi, baze, oxizi metalici, săruri ale acizilor slabi. De interes deosebit sunt interacțiunile aminoacizilor cu alcoolii care se referă la esterificare.

Caracteristici ale izomerismului
Pentru a înregistra formulele structurale ale aminoacizilor, observăm că mulți aminoacizi care participă la transformările biochimice conțin o grupare amino la poziția a din gruparea carboxil. Un astfel de atom de carbon este un centru chiral, iar aminoacizii sunt considerați izomeri optici.
Formula structurală a aminoacizilor dă o idee despre localizarea principalelor grupe funcționale conținute în substanță, în raport cu atomul de carbon activ.
Aminoacizii naturali, care fac parte din moleculele de proteine, sunt reprezentanți ai seriei L.
Pentru izomerii optici ai aminoacizilor, racemizarea spontană lentă non-enzimatică este caracteristică.

Caracteristicile compușilor a
Orice formula de substanțe de acest tip presupune dispunerea unei grupări amino la al doilea atom de carbon. 20 de aminoacizi, ale căror formule sunt considerate chiar și în cursul școlii de biologie, aparțin, de asemenea, acestei specii. De exemplu, ele includ alanină, asparagină, serină, leucină, tirozină, fenilalanină, valină. Acești compuși sunt cei care alcătuiesc codul genetic uman. Pe lângă conexiunile standard? de asemenea, în moleculele de proteine se găsesc aminoacizi nestandardi, care sunt derivații lor.
Clasificarea prin sinteză
Cum puteți separa aminoacizii esențiali? Formulele din această clasă sunt subdivizate pe baza fiziologiei în semne înlocuibile, capabile să fie sintetizate în corpul uman. Izolați și compușii obișnuiți, sintetizați în orice organism viu.

Diviziunea grupurilor radicale și funcționale
Formula de aminoacizi diferă în structura radicalului (grupul lateral). Există o diviziune în molecule nepolare care conțin un radical nonpolar hidrofob, precum și grupuri polar încărcate. Ca grup separat în biochimie, aminoacizii aromatici sunt considerați: histidină, triptofan, tirozină. În funcție de grupurile funcționale, se disting mai multe grupuri. Compușii alifatici sunt reprezentați de:
- compuși monoaminomonocarbonici, cum ar fi glicina, valina, alanina, leucina;
- substanțe hidroxinocaminocarbonice: treonină, serină;
- monoaminocarbon: glutamic, acid aspartic;
- compuși cu conținut de sulf: metionină, cisteină;
- substanțe diaminomonocarbonice: lizină, histidină, arginină;
- heterociclic: prolină, histidină, triptofan /
Orice formulă de aminoacizi poate fi scrisă într-o formă generală, numai grupurile radicale vor fi diferite.

Definiție calitativă
Pentru a detecta cantități mici de aminoacizi, se efectuează o reacție ninhidrină. În timpul încălzirii, aminoacizi cu un exces de ninhidrină se obține produsul mov, în cazul în care acidul are un liber un amino și o grupare protejată pentru prepararea produsului tipic galben. Această tehnică are o sensibilitate ridicată, este utilizată pentru detectarea colorimetrică a aminoacizilor. Pe baza sa, a fost elaborată o metodă de cromatografie prin distribuție pe hârtie, introdusă de Martin în 1944.
Aceeași reacție chimică este utilizată într-un analizor automat de aminoacizi. Dispozitivul creat de Moore, Shpakman, Stein, se bazează pe separarea amestecului de aminoacizi în coloanele care sunt umplute rășini schimbătoare de ioni. Din coloană, eluentul curge în mixer, iar aici vine ninhidrina.
Intensitatea culorii rezultate este evaluată pe baza conținutului cantitativ al aminoacizilor. Indicațiile fixează fotoelectrocolorimetrul, înregistratorul înregistrează.
Această tehnologie este utilizată în prezent în practica clinică pentru testele de sânge, lichidul cefalorahidian, urină. Acesta permite să ofere o imagine completă a compoziției calitative a aminoacizilor conținute în fluide biologice, pentru a determina în ele substanțe care conțin azot nestandard.
Caracteristicile nomenclatorului
Cât de corect să denumiți aminoacizii? Formulele și denumirile acestor compuși sunt date de nomenclatorul internațional al IUPAC. Poziția grupării amino este adăugată la acidul carboxilic corespunzător, începând cu numerotarea din hidrocarbură care se află sub gruparea carboxil.
De exemplu, acidul 2-aminoetanoic. În plus față de nomenclatura internațională, există nume triviale folosite în biochimie. Deci, acidul aminoacetic este glicina, utilizată în medicina modernă.
În prezența a două grupări carboxil în moleculă, sufixul sufix-dionic este adăugat la nume. De exemplu, acidul 2-aminobutandioic.
Toți membrii acestei clase sunt caracterizați prin izomerism structural, datorită schimbărilor în structura lanțului de carbon, precum și localizării grupărilor carboxil și amino. În plus față de glicină (cel mai simplu reprezentant al acestei clase de substanțe organice care conțin oxigen)? ceilalți compuși au antipoziți oglindă (izomeri optici).

cerere
Aminoacizii sunt de natură comună, ele constituie baza pentru construirea animalelor și a proteinelor vegetale. Acești compuși sunt utilizați în medicină în caz de epuizare severă a organismului, de exemplu, după operații chirurgicale complicate. Acidul glutamic ajută la combaterea bolilor nervoase, iar histidina este utilizată pentru a trata ulcerele de stomac. Când se sintetizează fibrele sintetice (acidul caproic, enantul), acidul aminocaproic și acidul aminoenantic acționează ca materie primă.
concluzie
Aminoacizii sunt compuși organici, care în compoziția lor au două grupe funcționale. Caracteristicile structurii explică dualitatea proprietăților lor chimice, precum și specificul utilizării lor. Conform rezultatelor experimentelor de cercetare, sa constatat că biomasa organismelor care trăiesc pe planeta noastră, pentru un total de 1,8 × 1012-2,4 × 1012 tone de substanță uscată vie. Aminoacizii sunt monomeri inițiali în biosinteza moleculelor de proteine, fără de care existența oamenilor și a animalelor este imposibilă.
În funcție de semnele fiziologice, există o subdiviziune a tuturor aminoacizilor în substanțe de neînlocuit, a căror sinteză nu se realizează în corpul uman și mamifere. Pentru a evita perturbările proceselor metabolice, este important să consumăm alimente în care există acești aminoacizi.
Acești compuși sunt "cărămizi" unice, care sunt folosite pentru a construi biopolimeri-proteine. În funcție de tipul reziduurilor de aminoacizi, în ce secvență se va construi structura proteinei, proteina formată are anumite proprietăți fizice și chimice și domenii de aplicare. Datorită reacțiilor calitative la grupurile funcționale, biochimii determină compoziția moleculelor de proteine și caută noi modalități de sintetizare a biopolimerilor individuali necesari organismului uman.
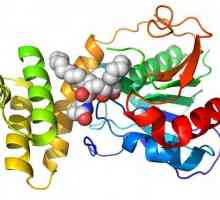 Rolul biologic al aminoacizilor și aplicarea lor
Rolul biologic al aminoacizilor și aplicarea lor Clasificarea substanțelor organice - baza pentru studiul chimiei organice
Clasificarea substanțelor organice - baza pentru studiul chimiei organice Proprietățile fizice ale aldehidelor
Proprietățile fizice ale aldehidelor Monomerii proteinelor sunt ce substanțe? Ce sunt monomeri de proteine?
Monomerii proteinelor sunt ce substanțe? Ce sunt monomeri de proteine? Proteine: clasificarea, structura și funcțiile proteinelor
Proteine: clasificarea, structura și funcțiile proteinelor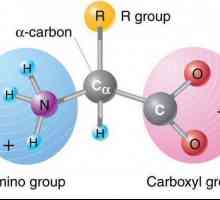 Histidină: formula, reacții chimice
Histidină: formula, reacții chimice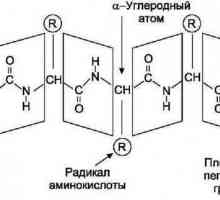 Din moleculele reziduurilor de aminoacizi ale celor construite?
Din moleculele reziduurilor de aminoacizi ale celor construite? Aminoacizi: biochimie, clasificare
Aminoacizi: biochimie, clasificare Proprietăți și funcții ale aminoacizilor
Proprietăți și funcții ale aminoacizilor Structura aminoacizilor. Determinarea și clasificarea aminoacizilor
Structura aminoacizilor. Determinarea și clasificarea aminoacizilor Proteină fibrilă și globulară, monomer proteic, tipare de sinteză a proteinelor
Proteină fibrilă și globulară, monomer proteic, tipare de sinteză a proteinelor Compuși organici și clasificarea acestora
Compuși organici și clasificarea acestora Nivelurile organizării structurale a moleculei proteice sau a structurii proteinei
Nivelurile organizării structurale a moleculei proteice sau a structurii proteinei Clase de compuși anorganici
Clase de compuși anorganici Hidrocarburi limită: caracteristici generale, izomerie, proprietăți chimice
Hidrocarburi limită: caracteristici generale, izomerie, proprietăți chimice Acid carboxilic
Acid carboxilic Seria de omologie
Seria de omologie Cele mai mari celule de materie organică
Cele mai mari celule de materie organică Structura primară a proteinei
Structura primară a proteinei Acizi dicarboxilici: descriere, proprietăți chimice, producție și aplicare
Acizi dicarboxilici: descriere, proprietăți chimice, producție și aplicare Compuși care conțin oxigen: exemple, proprietăți, formule
Compuși care conțin oxigen: exemple, proprietăți, formule
 Monomerii proteinelor sunt ce substanțe? Ce sunt monomeri de proteine?
Monomerii proteinelor sunt ce substanțe? Ce sunt monomeri de proteine? Proteine: clasificarea, structura și funcțiile proteinelor
Proteine: clasificarea, structura și funcțiile proteinelor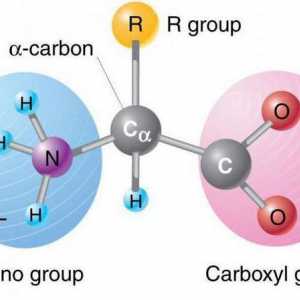 Histidină: formula, reacții chimice
Histidină: formula, reacții chimice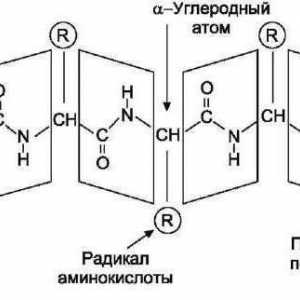 Din moleculele reziduurilor de aminoacizi ale celor construite?
Din moleculele reziduurilor de aminoacizi ale celor construite? Aminoacizi: biochimie, clasificare
Aminoacizi: biochimie, clasificare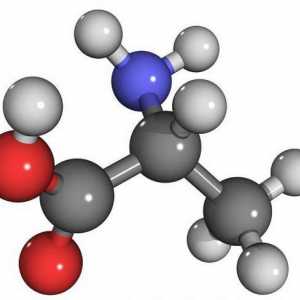 Proprietăți și funcții ale aminoacizilor
Proprietăți și funcții ale aminoacizilor Structura aminoacizilor. Determinarea și clasificarea aminoacizilor
Structura aminoacizilor. Determinarea și clasificarea aminoacizilor Proteină fibrilă și globulară, monomer proteic, tipare de sinteză a proteinelor
Proteină fibrilă și globulară, monomer proteic, tipare de sinteză a proteinelor